Nguyên tử là những phân tử cực kỳ nhỏ cấu trở thành nên đa số những dạng vật hóa học. Hạt nhân nguyên vẹn tử cướp một lượng đa số vô cấu trúc nguyên vẹn tử. Đây cũng là một trong những trong mỗi chủ thể phân tích cần thiết trong vô số nghành nghề dịch vụ lúc này. Hãy nằm trong VUIHOC lần hiểu kỹ rộng lớn về kỹ năng và kiến thức về phân tử nhân vô lịch trình Vật Lý 12.
Khái niệm phân tử nhân nguyên vẹn tử
Định nghĩa phân tử nhân nguyên vẹn tử

Bạn đang xem: Lý thuyết về hạt nhân nguyên tử
Hạt nhân nguyên vẹn tử là cấu hình vật hóa học đậm đặc (mật phỏng rất có thể lên tới mức 100 triệu tấn/cm3), cướp gần như là toàn cỗ lượng của nguyên vẹn tử. Theo một số trong những tư liệu được công tía lúc này thì độ cao thấp của phân tử nhân nguyên vẹn tử nằm trong một vùng số lượng giới hạn đem nửa đường kính khoảng tầm 10-15m.
Hạt nhân nguyên vẹn tử đem cấu trúc bao hàm những phân tử nào?
Hạt nhân nguyên vẹn tử đem cấu trúc kể từ 2 loại phân tử bao gồm:
Hạt Proton: Proton - theo dõi nghĩa giờ Hy Lạp tức là “thứ nhất”. Hạt Proton đem năng lượng điện +1 và đem lượng cực kỳ nhỏ, chỉ xấp xỉ vì như thế 1.67262158 × 10-27 kilogam (938.278 MeV/c2).
Hạt Nơtron: Đây là loại phân tử ko đem năng lượng điện và đem lượng chỉ tầm 1.67492716 × 10-27 kilogam (939.571 MeV/c2) và to hơn lượng của proton.
Một số lý thuyết tương quan cho tới phân tử nhân nguyên vẹn tử
Nguyên tố hóa học

Nguyên tố chất hóa học là những nguyên vẹn tử đem năng lượng điện phân tử nhân đều bằng nhau (có nằm trong Z). Tính cho tới thời gian thời điểm hiện tại, những mái ấm khoa học tập vẫn hiểu rằng cho tới 94 yếu tố chất hóa học đem vô đương nhiên và 24 yếu tố được loài người tạo nên kể từ những chống thử nghiệm phân tử nhân (tổng nằm trong đem tổng số 118 nguyên vẹn tố).
Ví dụ về yếu tố hóa học: Tất cả những nguyên vẹn tử đem đơn vị chức năng năng lượng điện phân tử nhân đều là 8 thì nằm trong yếu tố Oxi. Chúng tiếp tục bao hàm 8 proton và 8 electron
Số hiệu nguyên vẹn tử

Số hiệu nguyên vẹn tử chủ yếu thông qua số đơn vị chức năng năng lượng điện phân tử nhân của yếu tố cơ. Số hiệu nguyên vẹn tử đem ký hiệu là Z.
Ký hiệu nguyên vẹn tử
Những đặc thù cơ phiên bản nhất của nguyên vẹn tử đó là số đơn vị chức năng năng lượng điện phân tử nhân và số khối. Do cơ nhằm kí hiệu nguyên vẹn tử người tao hay được dùng những chỉ số đặc thù ở phía trái kí hiệu yếu tố X (số khối - ký hiệu là A - ở phía bên trên và số hiệu nguyên vẹn tử - ký hiệu là Z - ở phía dưới) đem dạng:
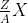
Ở hình hình họa ví dụ tao rất có thể thấy được số khối A của nguyên vẹn tử Natri là 23 và số hiệu nguyên vẹn tử Z là 11. Vì vậy tao rất có thể Tóm lại, số đơn vị chức năng năng lượng điện phân tử nhân của Na là 11 (có 11 proton và 11 electron) và bên phía trong phân tử nhân đem 12 notron.

Đồng vị
Các nguyên vẹn tử đem và một yếu tố chất hóa học ko nên khi này đem số khối giống như nhau và trọn vẹn rất có thể không giống nhau. tại sao của hiện tượng lạ này bởi phân tử nhân của nguyên vẹn tử tuy nhiên đem số proton giống như nhau tuy nhiên đem số nơtron không giống nhau.
Đồng vị của những yếu tố chất hóa học đem những nguyên vẹn tử giống như nhau về số proton tuy nhiên không giống nhau về số nơtron. Các đồng vị được xếp vô nằm trong 1 dù yếu tố vô bảng tuần trả yếu tố chất hóa học.
Xem thêm: Sử dụng sơ đồ Hoocne (Horner) để chia đa thức
Do đem số nơtron không giống nhau nhên số khối của những đồng vị cũng tiếp tục không giống nhau.
* Lưu ý: Cạnh ngoài đương nhiên có tầm khoảng 340 đồng vị, và những mái ấm khoa học tập còn tổ hợp tăng 2400 đồng vị tự tạo được dùng vô nông nghiệp và hắn học tập.
Ví dụ: Nguyên tố Hidro (H2) đem 3 đồng vị như sau:

Nguyên tử khối
Nguyên tử khối đó là lượng kha khá của một nguyên vẹn tử và cho biết thêm lượng của nguyên vẹn tử cơ nặng trĩu từng nào đợt đơn vị chức năng lượng nguyên vẹn tử.
Khối lượng của một nguyên vẹn tử được xem vì như thế tổng lượng của proton + nơtron + electron ở bên phía trong nguyên vẹn tử cơ. Nhưng do lượng của electron quá nhỏ đối với phân tử nhân nên thường thì lượng một nguyên vẹn tử được xem xấp xỉ vì như thế lượng phân tử nhân của nguyên vẹn tử cơ.
Vì vậy, nguyên vẹn tử khối được xem chủ yếu thông qua số khối (A).
Ví dụ: Xác toan nguyên vẹn tử khối của Phường hiểu được Phường đem N = 16 và Z = 15
Vậy nguyên vẹn tử khối của Phường là 31.
Nguyên tử khối trung bình
Ở vô đương nhiên, đem thật nhiều yếu tố chất hóa học tồn bên trên với rất nhiều đồng vị nên so với những yếu tố này, nguyên vẹn tử khối được xem vì như thế nguyên vẹn tử khối tầm của những đồng vị cơ.
Giả sử mang trong mình 1 yếu tố đem 2 đồng vị X và Y, X là nguyên vẹn tử khối ứng của đồng vị X và Y ứng là nguyên vẹn tử khối của đồng vị Y. a là tỷ lệ số nguyên vẹn tử của X và b là tỷ lệ số nguyên vẹn tử của Y. Từ cơ, tao đem công thức tính nguyên vẹn tử khối tầm của A là:

Đăng ký tức thì và để được những thầy cô tư vấn và xây đắp trong suốt lộ trình ôn ganh đua trung học phổ thông đạt 9+ sớm tức thì kể từ bây giờ

Trên đó là toàn cỗ kỹ năng và kiến thức về Hạt nhân nguyên vẹn tử vô lịch trình Vật Lý 12. Để tìm hiểu thêm tăng kỹ năng và kiến thức đáp ứng mang đến quy trình ôn ganh đua trung học phổ thông Quốc gia môn Vật Lý gần giống kỹ năng và kiến thức những môn học tập không giống, những em học viên rất có thể truy vấn vô website: framesi.com.vn. Chúc những em đạt được thành phẩm chất lượng tốt trong những kỳ ganh đua tiếp đây.
Xem thêm: Cách Chụp Ảnh Trên Tiktok Đơn Giản, Nhanh Nhất 2023 | Nguyễn Kim Blog
Tham khảo thêm:
Sơ lược về laze
Lý thuyết về phóng xạ





