Các kiến thức và kỹ năng về nguyên vẹn tử khối tầm rất rất cần thiết vì thế bọn chúng sẽ theo những em xuyên suốt 3 năm trung học phổ thông. thạo được vai trò cơ, VUIHOC đang được tổ hợp kiến thức và kỹ năng về nguyên vẹn tử khối tầm nằm trong cỗ bài bác luyện tự động luận rất rất hoặc và ý nghĩa sâu sắc. Các em nằm trong theo đuổi dõi nội dung bài viết sau đây nhé!
1. Các định nghĩa chi phí đề
1.1. Nguyên tử
Nguyên tử là đơn vị chức năng cơ bạn dạng của vật hóa học, bao hàm những phân tử trung hoà về năng lượng điện và sở hữu độ cao thấp siêu nhỏ. Nguyên tử sở hữu có một phân tử nhân ở trung tâm và được đám mây năng lượng điện âm electron phủ quanh.
Bạn đang xem: Nguyên tử khối trung bình: Công thức và mẹo xác định nhanh - VUIHOC Hoá học 10
Những nguyên vẹn tử thông thường đem độ cao thấp siêu nhỏ, 2 lần bán kính chỉ tầm vài ba phần chục của nano mét. Nguyên tử được kí hiệu là Z (Zahl theo đuổi giờ Đức)
Nguyên tử bao hàm phần phân tử nhân và lớp vỏ:
-
Hạt nhân: kết cấu kể từ 2 loại phân tử là proton (p) tích năng lượng điện dương (+) và notron (n) ko tích năng lượng điện.
-
Lớp vỏ: bao gồm những phân tử electron (e) tích năng lượng điện âm (-) vận động liên tiếp.
1.2. Nguyên tử khối
Nguyên tử khối là lượng kha khá của một loại nguyên vẹn tử.
Nguyên tử khối ký hiệu là (M) ngay số khối phân tử nhân: M = A
Nguyên tử khối của một nguyên vẹn tử mang lại tao biết lượng của nguyên vẹn tử cơ nặng trĩu cấp từng nào thứ tự đơn vị chức năng lượng nguyên vẹn tử. Đơn vị của nguyên vẹn tử khối
Khối lượng của nguyên vẹn tử vày tổng lượng của proton, nơtron và electron vô nguyên vẹn tử cơ. Proton và nơtron đều sở hữu lượng xấp xỉ 1u còn electron sở hữu lượng nhỏ rộng lớn thật nhiều, khoảng chừng 0,00055u. Do cơ, rất có thể coi nguyên vẹn tử khối xấp xỉ số khối của phân tử nhân.
Khối lượng của một nguyên vẹn tử vày lượng của những bộ phận kết cấu nên nguyên vẹn tử (proton, electron, nơtron) nhưng do vì phân tử electron sở hữu lượng quá nhỏ đối với tổng lượng nên coi lượng của phân tử electron vày 0. Vì vậy, Khi xét cho tới lượng nguyên vẹn tử, tao coi lượng nguyên vẹn tử vày tổng lượng phân tử proton và nơtron sở hữu vô phân tử nhân nguyên vẹn tử (mNT = mp + mn)
1.3. Đồng vị
Các nguyên vẹn tử của và một nhân tố chất hóa học rất có thể sở hữu số khối không giống nhau. Sở dĩ như thế vì thế phân tử nhân của những nguyên vẹn tử cơ sở hữu nằm trong số proton tuy nhiên rất có thể không giống số nơtron.
Các đồng vị của và một nhân tố chất hóa học là những nguyên vẹn tử sở hữu nằm trong số proton tuy nhiên không giống nhau về số nơtron, bởi vậy số khối A của bọn chúng không giống nhau.
Các đồng vị được xếp vô và một địa điểm (ô nguyên vẹn tố) vô bảng tuần trả.
Ví dụ: nhân tố Hidro sở hữu 3 đồng vị :
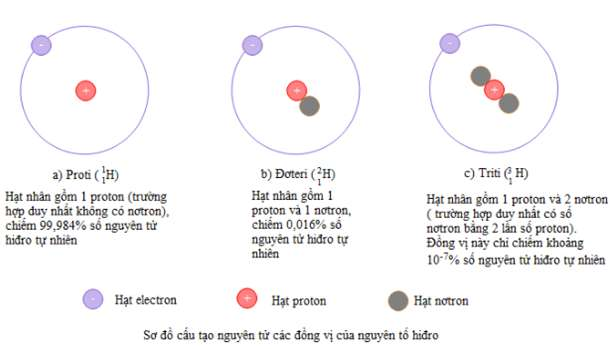
Đa số những nhân tố chất hóa học là láo lếu thích hợp của tương đối nhiều đồng vị không giống nhau. Ngoài khoảng chừng 340 đồng vị tồn bên trên vô đương nhiên, người tao đang được tổ hợp được 2400 đồng vị tự tạo. Các đồng vị của và một nhân tố chất hóa học sở hữu số nơtron vô phân tử nhân không giống nhau, nên sở hữu một vài đặc thù vật lí không giống nhau.
Ví dụ: Tại tình trạng đơn hóa học, đồng vị 3517Cl sở hữu tỉ số khối to hơn, nhiệt độ nhiệt độ chảy và nhiệt độ phỏng sôi cao hơn nữa đồng vị 3517Cl.
Người tao phân biệt những đồng vị bền và ko bền. Hầu không còn những đồng vị sở hữu số hiệu nguyên vẹn tử to hơn 83(Z > 83) là ko bền, bọn chúng còn được gọi là những đồng vị phóng xạ.
Nhiều đồng vị, nhất là những đồng vị phóng xạ, được dùng nhiều vô cuộc sống, nó học tập, nghiên cứu và phân tích sự cách tân và phát triển của cây cối.....
Đăng ký ngay lập tức sẽ được những thầy cô ôn luyện và thi công quãng thời gian học tập tập THPT vững vàng vàng

2. Nguyên tử khối trung bình
2.1. Định nghĩa nguyên vẹn tử khối trung bình
Hầu không còn những nhân tố chất hóa học là láo lếu thích hợp của tương đối nhiều đồng vị với tỉ lệ thành phần tỷ lệ số nguyên vẹn tử xác lập => nguyên vẹn tử khối của những nhân tố có tương đối nhiều đồng vị là nguyên vẹn tử khối tầm của láo lếu thích hợp những đồng vị sở hữu tính cho tới tỉ lệ thành phần tỷ lệ số nguyên vẹn tử ứng.
2.2. Công thức tính nguyên vẹn tử khối trung bình
M tầm = 
Với 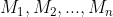 : nguyên vẹn tử khối (hay số khối) của những đồng vị
: nguyên vẹn tử khối (hay số khối) của những đồng vị
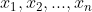 : số nguyên vẹn tử khối hoặc bộ phận số nguyên vẹn tử của những đồng vị
: số nguyên vẹn tử khối hoặc bộ phận số nguyên vẹn tử của những đồng vị
Xác tấp tểnh tỷ lệ những đồng vị
Gọi % của đồng vị một là x %
⇒ % của đồng vị 2 là (100 – x).
- Lập phương trình tính nguyên vẹn tử khối tầm ⇒ giải được x.
2.3. Một số ví dụ bài bác thói quen nguyên vẹn tử khối trung bình
Bài 1: Nguyên tố Cacbon sở hữu 2 đồng vị bền: 612C cướp 98,89% và 613C cướp 1,11%. Nguyên tử khối tầm của C là bao nhiêu?
M tầm = 12 x 98.89 + 13 x 1.11100 = 12.0111
Vậy nguyên vẹn tử khối tầm của C là 12,0111
3. Bài thói quen nguyên vẹn tử khối trung bình
Bài 1: Trong đương nhiên, X sở hữu nhì đồng vị 1735X và 1737X, cướp theo lần lượt 75,77% và 24,23% số nguyên vẹn tử X. Y sở hữu nhì đông đúc vị à 11Y và 12Y, cướp theo lần lượt 99,2% và 0,8% số nguyên vẹn tử Y.
a) Trong đương nhiên sở hữu từng nào loại phân tử XY?
b) Phân tử khối tầm của XY là bao nhiêu?
c) Phân tử XY là hóa học nào?
Hướng dẫn giải chi tiết
a) Các loại phân tử XY là : 35X – 1Y, 35X – 2Y, 37X – 1Y, 37X – 2Y
b) Nguyên tử khối tầm của X là : 75.77 x 35 + 24.23 x 37100 = 35.485
Nguyên tử khối tầm Y là: 99.2 x 1 + 0.8 x 2100 = 1.008
Phân tử khối tầm của XY: 35,485 + 1,008 =36,493 ≈ 36,5.
c) Phân tử XY là HCl
Bài 2: Cho thích hợp hóa học AB2 tạo nên vày nhì nhân tố A, B. B sở hữu nhì đồng vị 79B: cướp 55% số nguyên vẹn tử B và đồng vị 81B. Trong AB2, tỷ lệ lượng của A là vày 28,51%. Tính nguyên vẹn tử khối tầm của A, B.
Hướng dẫn giải chi tiết
Giải quí công việc giải:
Phần trăm số nguyên vẹn tử của 81B = 100%−55% = 45%
Suy rời khỏi, nguyên vẹn tử khối tầm của B là :
MB= 79.55% + 81.45% = 79,9
Ta có
% A= (A/A + 2B).100% = (A/B + 79,9.2).100% = 28,51%
⇒ A = 63,73
Bài 3: Nguyên tố clo sở hữu nhì đồng vị bền 1735 Cl cướp 75,77% và 1737 Cl cướp 24,23%. Tính nguyên vẹn tử khối trung của Clo?
Hướng dẫn giải chi tiết
Nguyên tử khối tầm của Clo là: 35 x 75.77 + 37 x 24.23100 = 35.5
Xem thêm: NaOH + H2SO4 → Na2SO4+ H2O.
Vậy nguyên vẹn tử khối tầm của Clo là 35.5
Bài 4: Nguyên tử khối tầm của đồng là 63,54. Trong đương nhiên, đồng sở hữu nhì đồng vị 6329Cu và 6529Cu Tính tỉ lệ thành phần tỷ lệ số nguyên vẹn tử của đồng vị 2963Cu tồn bên trên vô tự động nhiên
Hướng dẫn giải chi tiết
Gọi x là % số nguyên vẹn tử của2963Cu ⇒ 100 – x là % của 2965Cu
Ta sở hữu 63,54 = (63x + 65)(100 - x))/100 ⇒ x = 73
Vậy 2963Cu cướp 73%
Bài 5: Trong đương nhiên Oxi sở hữu 3 đồng vị 16O(x1%), 17O(x2%), 18O (4%), nguyên vẹn tử khối tầm của Oxi là 16,14. Phần trăm đồng vị 16O và 17O theo lần lượt là bao nhiêu?
Hướng dẫn giải chi tiết
Ta có: x1 + x2 + 4 = 100
Nguyên tử khối tầm của Oxi là 16.14 = (16. x1 + 17. x2 + 18.4)/100
Giải hệ phương trình 2 ẩn tao sở hữu x1 = 90 và x2 = 6
Bài 6: Một nhân tố X bao gồm nhì đồng vị là X1 và X2. Đồng vị X1 sở hữu tổng số phân tử là 18. Đồng vị X2 sở hữu tổng số phân tử là trăng tròn. thạo rằng % những đồng vị vô X đều nhau và những loại phân tử vô X1 cũng đều nhau. Xác tấp tểnh nguyên vẹn tử khối tầm của X?
Hướng dẫn giải chi tiết
Các phân tử vô đồng vị X1 đều nhau nên: P.. = E = N = 18/3 = 6
⇒ Số khối của đồng vị X1 là: P.. + N= 12
⇒ Số khối của đồng vị X2 là: trăng tròn – 6 = 14
M tầm = 35 x 75.77 + 37 x 24.23100 = 13
Bài 7: Nguyên tử khối tầm của đồng là 63,54. Trong đương nhiên, đồng sở hữu nhì đồng vị Cu2963 và Cu2965 Tính tỉ lệ thành phần tỷ lệ số nguyên vẹn tử của đồng vị Cu2963 tồn bên trên vô đương nhiên.
Hướng dẫn giải chi tiết
Gọi x là % số nguyên vẹn tử của Cu2963 ⇒ 100 – x là % của Cu2965
Ta sở hữu 63,54 = (63x + 65(100 - x))/100 ⇒ x = 73
Vậy Cu2963chiếm 73%
Bài 8: Biết lượng của nguyên vẹn tử cacbon 12 cấp 11,9059 thứ tự lượng của nguyên vẹn tử hiđro. Hỏi lượng của nguyên vẹn tử hiđro vày từng nào u?
Hướng dẫn giải chi tiết
Khối lượng nguyên vẹn tử hidro là: 1211.9059 = 1.0079
Bài 9: Một nguyên vẹn tử x bao gồm 2 đồng vị là x1 và x2, theo lần lượt sở hữu tổng số phân tử là 15 và 18. thạo rằng % của những đồng vị vô X đều nhau và những loại hoạt vô X1 cũng vày cùng nhau. Hãy xác lập nguyên vẹn tử khối tầm của X là bao nhiêu?
Hướng dẫn giải chi tiết
Những phân tử vô đồng vị X1 đều nhau nên tao có:
P = E = N = 15/3 = 5
→ Số khối của đồng vị X1 là: P.. + N = 5 + 5 = 10
→ Số khối của đồng vị X2 là 18 – 5 = 13
Nguyên tử khối tầm của X là 575.
Bài 10: Cacbon sở hữu nhì đồng vị bền là C612và C613, và Số khối của cacbon = 12,01. Tính % lượng của vô thích hợp hóa học CO2 (cho MNa = 23; MO = 16)
Hướng dẫn giải chi tiết
Gọi a, b theo lần lượt là % số nguyên vẹn tử của đồng vị 12C và 13C
Ta lập được hệ phương trình sau
a + b = 100 (1)
12a/100 + 13b/100 = 12,01 (2)
Giải hệ phương trình bên trên tao được a = 99, b = 1
Xét 1 mol CO21 mol C => mC= 12,01
2 mol O => mO = 32
Ta biết % số nguyên vẹn tử = % số mol nên
Số mol của 12C là: 0,99.1 = 0,99 mol
%m12C = (0,99.12.100)/(12,01+ 32) = 27
PAS VUIHOC – GIẢI PHÁP ÔN LUYỆN CÁ NHÂN HÓA
Khóa học tập online ĐẦU TIÊN VÀ DUY NHẤT:
⭐ Xây dựng quãng thời gian học tập kể từ mất mặt gốc cho tới 27+
⭐ Chọn thầy cô, lớp, môn học tập theo đuổi sở thích
⭐ Tương tác thẳng hai phía nằm trong thầy cô
⭐ Học đến lớp lại cho tới lúc nào hiểu bài bác thì thôi
⭐ Rèn tips tricks hùn bức tốc thời hạn thực hiện đề
⭐ Tặng full cỗ tư liệu độc quyền vô quy trình học tập tập
Xem thêm: Lệnh tính diện tích trong Cad đơn giản, đầy đủ nhất
Đăng ký học tập test free ngay!!

Muốn học tập đảm bảo chất lượng hoá học tập thì trước không còn những em nên dò xét hiểu kể từ dạng bài bác luyện về nguyên tử khối trung bình. thạo được vai trò của công thức nguyên vẹn tử khối tầm, VUIHOC đang được ghi chép nội dung bài viết này nhằm mục đích gia tăng lý thuyết về cấu hình nguyên vẹn tử kèm cặp cỗ bài bác luyện rất rất có lợi. Để học tập thêm thắt được rất nhiều những kiến thức và kỹ năng hoặc và thú vị về Hoá học tập 10 rưa rứa Hoá học tập trung học phổ thông thì những em hãy truy vấn framesi.com.vn hoặc ĐK khoá học tập với những thầy cô VUIHOC ngay lập tức giờ đây nhé!

